衛材株式會社將在第15屆阿爾茨海默病臨床試驗(CTAD)會議上介紹侖卡奈單抗(lecanemab,開發代碼:BAN2401)Clarity AD III期驗證性臨床試驗的療效、安全性和生物標志物結果,試驗藥物侖卡奈單抗是治療腦內確認存在淀粉樣蛋白病理的阿爾茨海默病(AD)所致輕度認知障礙(MCI)和輕度AD(統稱為早期AD)的抗淀粉樣蛋白 (Aβ) 原纖維抗體。會議將于11月29日至12月2日在加州舊金山舉行,衛材和相關研究人員將在會議第一天的科學會議上展示全部數據(11月29日下午4:50 PT)。此外,來自侖卡奈單抗臨床開發項目和衛材AD管線的其它重要研究,包括該公司正在研究的抗微管結合區(MTBR)tau抗體(E2814),將通過四個演講展示和十個海報展示進行介紹。
Clarity AD的頂線(TOPLINE)結果已于9月下旬公布,顯示侖卡奈單抗符合主要終點和所有關鍵次要終點,結果具有高度統計學意義,淀粉樣蛋白相關成像異常(ARIA)發生率在預期范圍內。
衛材在CTAD上侖卡奈單抗主要報告:
- Clarity AD:在11月29日下午4:50 PT的科學會議上,將公布侖卡奈單抗用于早期AD患者的III期驗證性AD臨床試驗全部結果。衛材將對會議演講進行網絡直播,并可在衛材株式會社網站的投資者欄目中觀看直播。
- Aβ原纖維的結合特性:研究Aβ原纖維的特性以及侖卡奈單抗的獨特結合特性和Aβ清除機制(海報#P029)。
- AHEAD 3-45研究。
o 評估來自AHEAD 3-45期研究的侖卡奈單抗的tau PET篩選數據與血漿p-tau217和認知測試的關聯(Late Breaker Oral #LB1)。
o 利用AHEAD 3-45研究的3期篩查數據中的Abeta42/40和p-tau217比值的血漿水平,探索提高臨床前AD中淀粉樣蛋白PET預測的準確性(Late Breaker Oral #LB2)。
衛材株式會社阿爾茨海默病和腦健康首席臨床官、醫學博士Lynn Kramer 表示,“根據Clarity AD的結果,正在研究的抗淀粉樣蛋白β原纖維抗體侖卡奈單抗有可能通過減緩認知和功能衰退,對阿爾茨海默病早期患者及其家人產生臨床意義的影響。衛材很高興在CTAD上分享公司的驗證性III期Clarity AD臨床研究的結果,并展示探索侖卡奈單抗有效性、安全性和在各種早期AD患者亞群中的潛在使用的重要數據。”
CTAD 2022 Presentations Relating to Eisai's Key Compounds, Research and Collaborations

Oral Presentations
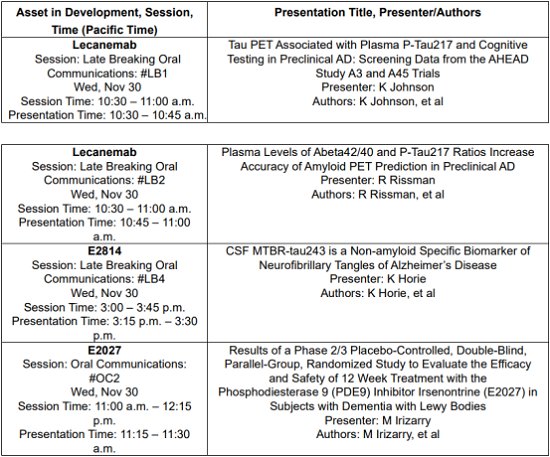
Poster Presentations
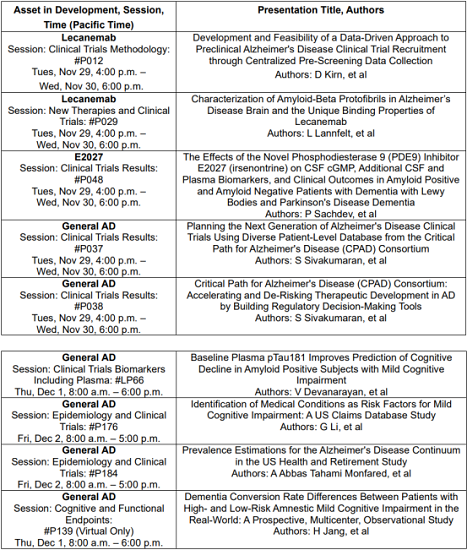
Sysmex Poster Presentation
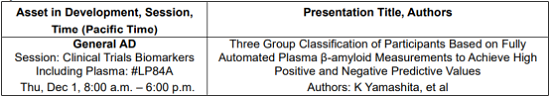
衛材預計在2022財年結束前(截至2023年3月31日)完成美國傳統審批程序和在日本和歐洲的上市許可申請。2022年7月,美國食品藥品監督管理局(FDA)受理了衛材侖卡奈單抗在快速通道認定下的生物制品許可申請(BLA),并授予優先審查權。處方藥用戶費用法案的行動(PDUFA)日期定于2023年1月6日。FDA已同意Clarity AD的結果作為驗證性研究來支持侖卡奈單抗的臨床獲益。為了盡快確保FDA對侖卡奈單抗的批準,衛材通過FDA的加速批準途徑提交了BLA,以便該機構可以提前完成對驗證性Clarity AD研究外的侖卡奈單抗全部數據的審查。2022年3月,衛材開始在事前評估咨詢系統下向日本藥品和醫療器械局(PMDA)提交除Clarity AD數據外的申請,目的是能夠盡早獲得侖卡奈單抗的批準,以便早期AD患者能盡快接受治療。
侖卡奈單抗的全球開發和監管提交由衛材主導,而產品則由衛材和渤健共同商業化和推廣,其中衛材擁有最終決策權。
本發布內容討論了藥物在開發中的研究用途,并非旨在傳達有關療效或安全性的結論。無法保證此類研究藥物將成功完成臨床開發或獲得衛生監管當局的批準。
免責聲明:市場有風險,選擇需謹慎!此文僅供參考,不作買賣依據。
關鍵詞:
版權與免責聲明:
1 本網注明“來源:×××”(非商業周刊網)的作品,均轉載自其它媒體,轉載目的在于傳遞更多信息,并不代表本網贊同其觀點和對其真實性負責,本網不承擔此類稿件侵權行為的連帶責任。
2 在本網的新聞頁面或BBS上進行跟帖或發表言論者,文責自負。
3 相關信息并未經過本網站證實,不對您構成任何投資建議,據此操作,風險自擔。
4 如涉及作品內容、版權等其它問題,請在30日內同本網聯系。